Woda królewska (łac. aqua regia) jest mieszaniną dwóch mocnych kwasów nieorganicznych – kwasu azotowego (V) oraz kwasu chlorowodorowego (solnego) w stosunku 1:3. Ma bardzo silne działanie utleniające. Jest w stanie reagować z metalami szlachetnymi, takimi jak złoto czy platyna oraz metalami opornymi chemicznie (m.in. molibden, cyrkon). Jej masa molowa wynosi 172.39 g/mol.
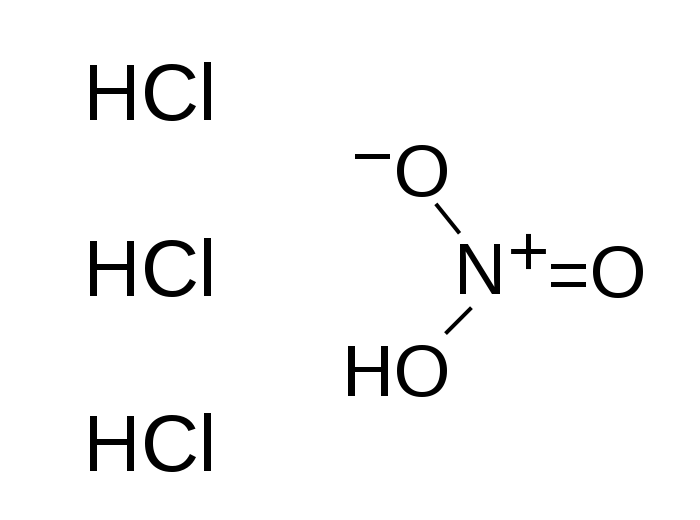
https://commons.wikimedia.org/wiki/File:Aqua_regia.svg
Woda królewska jest żółto-pomarańczową cieczą i tak samo jak czysty kwas azotowy (V), wytwarza na powierzchni brunatny gaz o duszącym zapachu tj. tlenek azotu (IV). Barwa wody królewskiej pochodzi od chlorku nitrozylu (NOCl).
Reakcja zachodząca w roztworze pomiędzy dwoma kwasami ma postać:
3HCl + HNO3 → Cl2 + NOCl + 2H2O
Woda królewska reaguje egzotermicznie z wodorotlenkami i aminami, tworząc ich sole. Może być czynnikiem inicjującym polimeryzację związków organicznych. Reaguje z solami cyjankowymi, tworząc toksyczny gazowy cyjanowodór. Reakcjom metali z wodą królewską towarzyszy wydzielanie toksycznych, a często i łatwopalnych gazów.
Podczas reakcji z metalami czynnikiem utleniającym w wodzie królewskiej jest kwas azotowy (V). Aniony chlorkowe pełnią funkcję kompleksującą - łączy się z powstałymi kationami metali:
Au + 3NO3- + 6H+ → Au3+ + 3NO2↑ + 3H2O,
Au3+ + 4Cl- → [AuCl4]-
Dawniej woda królewska służyła do oczyszczania szkła laboratoryjnego z osadów metalicznych i organicznych.
Woda królewska Wasze opinie
W tym temacie przypomniała mi się anegdota, którą dawno temu opowiadała bliska znajoma, śp. Pani Aldonka. Otóż na pewnej uczelni podczas egzaminu, profesor zasiał panikę wśród części studentów, zadając pytanie: "czy król może korzystać ze złotego nocnika"?
Czy woda królewska to nie mieszanka kwasu azotowego z siarkowym?