Historia układu okresowego rozpoczyna się w momencie, gdy zaczęto podejmować próby oddzielenia wierzeń alchemicznych od wiedzy chemicznej, co w rezultacie przyniosło pierwsze podwaliny chemii nowożytnej. Pierwszym naukowcem, któremu można przyznać zasługi w tym procesie, jest brytyjski fizyk i chemik Robert Boyle, który w połowie XVII w. opublikował książkę na temat budowy materii. Stwierdził on, że wszystkie obiekty fizyczne składają się z pewnych cząstek elementarnych, a obserwowane zjawiska są wynikiem zderzeń tych cząstek ze sobą. Boyle zawarł w pracy również listę 15 pierwiastków chemicznych i zastrzegł, że jest ich prawdopodobnie zdecydowanie więcej. Książka ta stała się początkiem ich systematyki.
Po 100 latach francuski chemik Antoine Lavoisier wyróżnił już ok. 35 pierwiastków chemicznych. Podzielił też dotychczas poznane związki chemiczne na gazy, niemetale, metale oraz ziemie (czyli tlenki).
Na początku XIX w. naukowcy znali już ok. połowę pierwiastków, które dzisiaj widnieją w układzie okresowym, dlatego dostrzeżenie pewnego podobieństwa pomiędzy nimi było dość trudne. Przypuszcza się, że pierwszym naukowcem, który podjął próbę pogrupowania pierwiastków w zależności od ich właściwości, był Johann Wolfgang Döbereiner. Zauważył on, że jeśli pogrupuje się pierwiastki na podstawie ich właściwości chemicznych, to dane grupy będą wykazywały również podobieństwo we właściwościach fizycznych (tj. masach atomowych). Tak powstały tzw. triady Döbereinera.
Z upływem czasu poznawano i opisywano nowe pierwiastki chemiczne i konstruowano kolejne modele systematyczne. W 1863 r. francuski geolog Alexandre-Émile Béguyer de Chancourtois opracował tzw. „śrubę telluryczną” (lub „bęben pierwiastków”). Schemat ten miał postać szeregu pierwiastków, ułożonych w kolejności wzrastającej masy atomowej, umiejscowionych na helisie. Spirala była tak skonstruowana, że jeden obrót przypadał co osiem pierwiastków. System ten nie zyskał jednak popularności.
Kolejnym uczonym, którego odkrycia przybliżyły świat naukowy do skonstruowania układu okresowego, był brytyjski chemik John Newlands. Sformułował on prawo okresowości dotyczące pierwiastków chemicznych, które nazwał prawem oktawy. Stwierdził w nim, że w szeregu pierwiastków ułożonych zgodnie ze wzrastającą masą atomową, co ósmy ma podobne właściwości. Nie wziął on jednak pod uwagę, że nie odkryto jeszcze wszystkich pierwiastków i wiele z nich nie wpisywało się (jeszcze) w sformułowaną przez niego tezę.
Przełomową pracą w systematyce pierwiastków chemicznych było skonstruowane przez rosyjskiego chemika Dmitrija Mendelejewa i opublikowane w 1869 r. zestawienie 90 z nich. Praca ta wyróżniała się na tle pozostałych lukami pozostawionymi w miejscach, gdzie występowały zbyt duże różnice pomiędzy znanymi molekułami. Tak Mendelejew przewidział istnienie 8 pierwiastków chemicznych.
Biorąc pod uwagę wiedzę, jaką dysponowali ówcześni chemicy, obserwacje dokonane do końca XIX w. na temat zależności pomiędzy pierwiastkami chemicznymi były niezwykłe. Należy pamiętać, że nie zdawano sobie wtedy sprawy, jak tak naprawdę wygląda atom i że nie jest on cząstką niepodzielną.
Dopiero początek XX w. przyniósł przełom w tym zakresie. Wtedy to w 1911 r. Ernest Rutherford odkrył jądro atomowe, a w 1913 r. jego uczeń Henry Moseley opublikował tabelę z liczbami protonów, neutronów i elektronów, budujących kolejne pierwiastki. Odkrycie Moseleya pokrywało się z teorią Nielsa Bohra na temat modelu atomu pierwiastka. Pozwoliło to na uaktualnienie układu okresowego, przez ułożenie pierwiastków nie według rosnących liczb masowych a atomowych (liczby protonów w jądrze). Tak skonstruowany układ jest niezmieniany od prawie 100 lat (pomijając luki, które zostały w kolejnych latach wypełnione nowo poznanymi pierwiastkami i wydzielenia grup lantanowców i aktynowców).
Ostatni pierwiastek, którego istnienie przewidział Mendelejew, został odkryty w 1936 r. przez zespół włoskich uczonych.
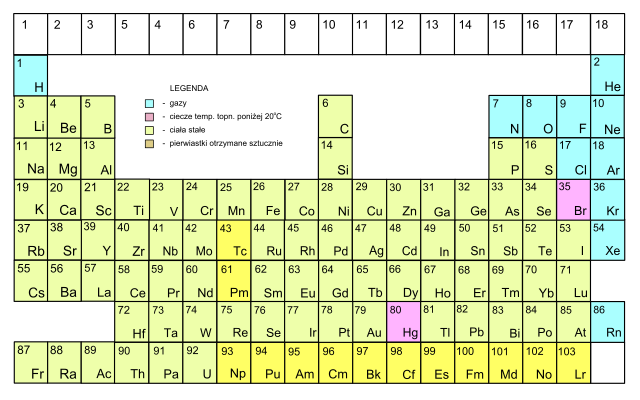
Historia układu okresowego pierwiastków Wasze opinie