1. Wzór sumaryczny
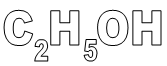 2. Wzór strukturalny
2. Wzór strukturalny
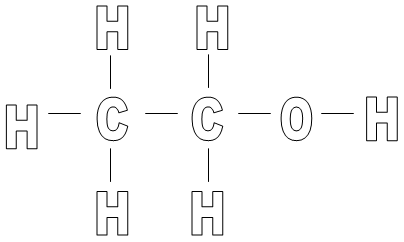 3. Właściwości
3. Właściwości
Masa molowa: 46,07 g/mol
Gęstość : 0,7893 g/cm3
pH: obojętne
Temperatura wrzenia: 78°C
Temperatura topnienia: -114°C
Temperatura samozapłonu: 425°C
Temperatura zapłonu: 17°C
Rozpuszczalność:
w wodzie: rozpuszczalny
w rozpuszczalnikach organicznych: rozpuszczalny
Etanol jest bezbarwną cieczą, bardziej lotną od wody o charakterystycznym zapachu. W swojej cząsteczce zawiera silnie polarną grupę –OH, dzięki czemu bardzo dobrze rozpuszcza się w wodzie, miesza się z nią w każdych proporcjach. Spala się jasnoniebieskim płomieniem, w wyniku czego powstaje woda i dwutlenek węgla:
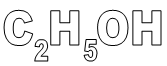 2. Wzór strukturalny
2. Wzór strukturalny 3. Właściwości
3. WłaściwościMasa molowa: 46,07 g/mol
Gęstość : 0,7893 g/cm3
pH: obojętne
Temperatura wrzenia: 78°C
Temperatura topnienia: -114°C
Temperatura samozapłonu: 425°C
Temperatura zapłonu: 17°C
Rozpuszczalność:
w wodzie: rozpuszczalny
w rozpuszczalnikach organicznych: rozpuszczalny
Etanol jest bezbarwną cieczą, bardziej lotną od wody o charakterystycznym zapachu. W swojej cząsteczce zawiera silnie polarną grupę –OH, dzięki czemu bardzo dobrze rozpuszcza się w wodzie, miesza się z nią w każdych proporcjach. Spala się jasnoniebieskim płomieniem, w wyniku czego powstaje woda i dwutlenek węgla:
\(C_2H_5OH + 3 O_2 \rightarrow 2CO_2 + 3H_2O\)
Alkohole z reguły są bardzo słabymi kwasami. O kwasowej własności etanolu świadczy między innymi powstanie etanolanu sodu w reakcji etanolu z aktywnym metalem, w tym przypadku sodem:
\(2 C_2H_5OH + 2 Na \rightarrow C_2H_5ONa + H_2\)
Etanol pod względem kwasowości jest porównywalny z wodą, ilustrują to ich wartości pKa, dla wody wynosi ona 15,7 zaś dla etanolu 15,9.
Pod względem własności zasadowych etanol również porównuje się z wodą, ponieważ tak jak ona zawiera wolne pary elektronów przy atomach tlenu. Przyłączenie protonu do cząsteczki etanolu wytwarza jon etylooksoniwy:
Pod względem własności zasadowych etanol również porównuje się z wodą, ponieważ tak jak ona zawiera wolne pary elektronów przy atomach tlenu. Przyłączenie protonu do cząsteczki etanolu wytwarza jon etylooksoniwy:
\(C_2H_5O–OH + H^+ ↔ C_2H_{5^-}+ \: ^+OH_2\)
4. Otrzymywanie
W przemyśle alkohol etylowy najczęściej otrzymuje się w wyniku fermentacji . Fermentacją nazywamy złożony proces przetworzenia w alkohol niektórych cukrów zawartych w roślinach (mogą to być cukry wydzielane z owoców, kukurydzy czy zboża). Przetworzenie to wymaga obecności drożdży, które są źródłem enzymów katalizujących cały proces. W sposób ogólny fermentacja etanolu przebiega następująco:
• Skrobia pod wpływem enzymu diastazy (biokatalizator znajdujący się w kiełkującym jęczmieniu) hydrolizuje na dicukier maltozę
• Skrobia pod wpływem enzymu diastazy (biokatalizator znajdujący się w kiełkującym jęczmieniu) hydrolizuje na dicukier maltozę
\(2 (C_6H_{10}O_5)_n + n H_2O \rightarrow n C_{12}H_{22}O_{11}\)
skrobia maltoza
• Maltoza z kolei hydrolizuje na dwie cząsteczki glikozy, przy czynnym współdziałaniu maltazy, enzymu znajdującego się w drożdżach:
\(C_{12}H_{22}O_{11} + H_2O \rightarrow 2 C_6H_{12}O_6\)
maltoza glikoza
• Trzeci enzym – zymaza – znajdujący się również w drożdżach, katalizuje rozkład glikozy na dwie cząsteczki etanolu i dwie cząsteczki dwutlenku węgla:
• Trzeci enzym – zymaza – znajdujący się również w drożdżach, katalizuje rozkład glikozy na dwie cząsteczki etanolu i dwie cząsteczki dwutlenku węgla:
\(C_6H_{12}O_6 \rightarrow 2 C_2H_5OH + 2 CO_2\)
Duże ilości alkoholu etylowego otrzymuje się w przemyśle, przez przyłączenie wody do etylenu. Reakcja przebiega pod zwiększonym ciśnieniem, w temperaturze 573 K, wobec kwasu fosforowego:
\(C_2H_4 + H_2O \xrightarrow[573K]{H_3PO_4} C_2H_5OH\)
W chemii etanol można otrzymać różnymi metodami, może to być na przykład addycja wody do etenu lub substytucja chlorowca w chloroetanie. Poniższe reakcje prezentują niektóre z metod:
\(C_2H_5Cl + NaOH \xrightarrow{H_2O} C_2H_5OH + NaCl\)
\(C_2H_4 + H_2O \xrightarrow{H^+} C_2H_5OH\)
\(C_2H_4 + H_2O \xrightarrow{H^+} C_2H_5OH\)
Substancją wyjściową do otrzymywania alkoholi są często estry. Poprzez ich redukcję możemy również otrzymać alkohol etylowy:
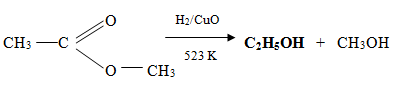

5. Zastosowanie
Alkohol etylowy ma różnorodne zastosowanie. Roztwory etanolu stosowane są jako napoje odurzające, które mogą prowadzić do uzależnienia. Etanol stosuje się również jako paliwo, ponieważ pali się jasnym niekopcącym płomieniem, wydzielając przy tym dużo ciepła. Jest również bardzo dobrym rozpuszczalnikiem, stosowany do wyrobu lakierów bądź perfum oraz jako środek dezynfekcyjny i konserwujący. Może być również stosowany jako surowiec wyjściowy do otrzymywania syntetycznego kauczuku, eteru i kwasu octowego. Spore ilości alkoholu etylowego, po zabarwieniu i skażeniu(najczęściej zasadami pirydynowymi), zużywa się do celów opałowych (denaturat).
6. Metabolizm etanolu
Metabolizm alkoholu etylowego w organizmie człowieka zachodzi głównie w wątrobie ale również w mózgu. Etanol utleniany jest do aldehydu octowego. W mózgu występują trzy układy utleniające etanol, a są to: dehydrogenaza alkoholowa (ADH), cytochrom P450 2E1 oraz katalaza. Dominującą rolę w przemianach alkoholu etylowego w mózgu w przypadku krótkotrwałego, rzadkiego spożycia odgrywają dwa z nich: ADH oraz katalaza. Jednak w przypadku długotrwałego, systematycznego podawania dużych dawek. Główną rolę w procesie oksydacji pełni cytochrom P450 2E1.
6. Metabolizm etanolu
Metabolizm alkoholu etylowego w organizmie człowieka zachodzi głównie w wątrobie ale również w mózgu. Etanol utleniany jest do aldehydu octowego. W mózgu występują trzy układy utleniające etanol, a są to: dehydrogenaza alkoholowa (ADH), cytochrom P450 2E1 oraz katalaza. Dominującą rolę w przemianach alkoholu etylowego w mózgu w przypadku krótkotrwałego, rzadkiego spożycia odgrywają dwa z nich: ADH oraz katalaza. Jednak w przypadku długotrwałego, systematycznego podawania dużych dawek. Główną rolę w procesie oksydacji pełni cytochrom P450 2E1.
Alkohol etylowy Wasze opinie