Przemianą termodynamiczną nazywana jest zmiana stanu układu termodynamicznego. W zależności od tego, jak zmieniają się funkcje stanu układu, można wyróżnić różne rodzaje przemian termodynamicznych.
Przemianą, w której ciśnienie \(p\) nie ulega zmianie (\(p=const.\)) nazywana jest przemianą izobaryczną. Na poniższym wykresie \(p(V)\) przedstawiono taką przemianę. Zgodnie z teorią gazu doskonałego, w przemianie izobarycznej stały pozostaje stosunek objętości do temperatury:
\(\dfrac{V}{T} = const.\)
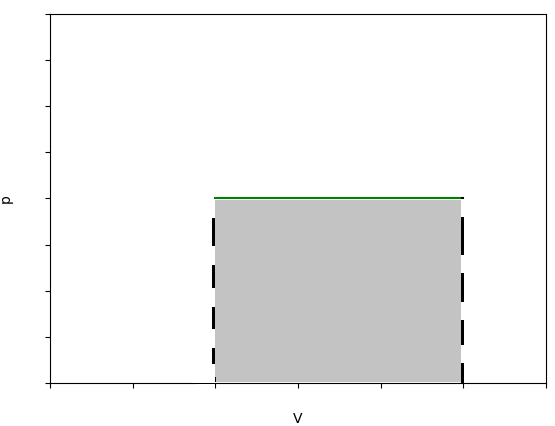
Pole pod wykresem jest równe wykonanej pracy \(W = p\cdot \Delta V\) przy ciśnieniu \(p\) i zmianie objętości \(\Delta V\).
Przemianą, w której objętość \(V\) nie ulega zmianie (\(V=const.\)) nazywana jest przemianą izochoryczną. Zgodnie z teorią gazu doskonałego, w przemianie izobarycznej stały pozostaje stosunek ciśnienia do temperatury:
\(\dfrac{p}{T} = const.\)
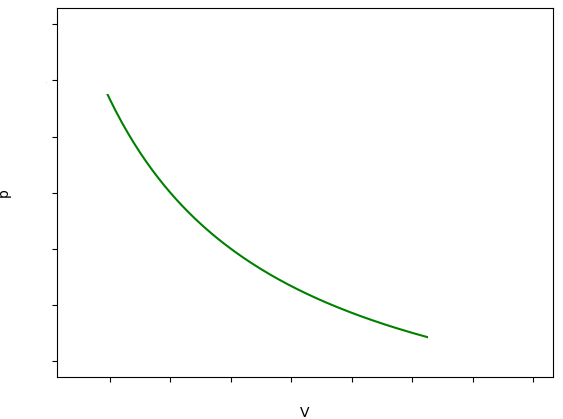
Przemianą, w której temperatura \(T\) nie ulega zmianie (\(T=const.\)) nazywana jest przemianą izotermiczną. Zgodnie z teorią gazu doskonałego, w przemianie izobarycznej stały pozostaje iloczyn ciśnienia i objętości:
\(p\cdot V = const.\)
Na wykresie poniżej przedstawiono taką przemianę.
Przemianę, w której nie ma wymiany ciepła z otoczeniem nazywa się przemianą adiabatyczną. Jej wykresem jest adiabata, opisana równaniem:
\(p\cdot V^\kappa = const.\) gdzie \(\kappa=\dfrac{c_p}{c_v}\) jest stosunkiem ciepła właściwego przy stałym ciśnieniu, do ciepła właściwego przy stałej objętości.
Wykresem przemiany izotermicznej jest izoterma, izobarycznej - izobara, a izochorycznej - izochora.
Przemiany termodynamiczne Wasze opinie