Aldehydy i ketony to organiczne związki chemiczne kwalifikowane do związków karbonylowych tj. posiadających w swej budowie grupę karbonylową (-C=O). Poza nimi do karbonyli należą również kwasy karbonylowe i ich pochodne (estry, chlorki, amidy, bezwodniki).
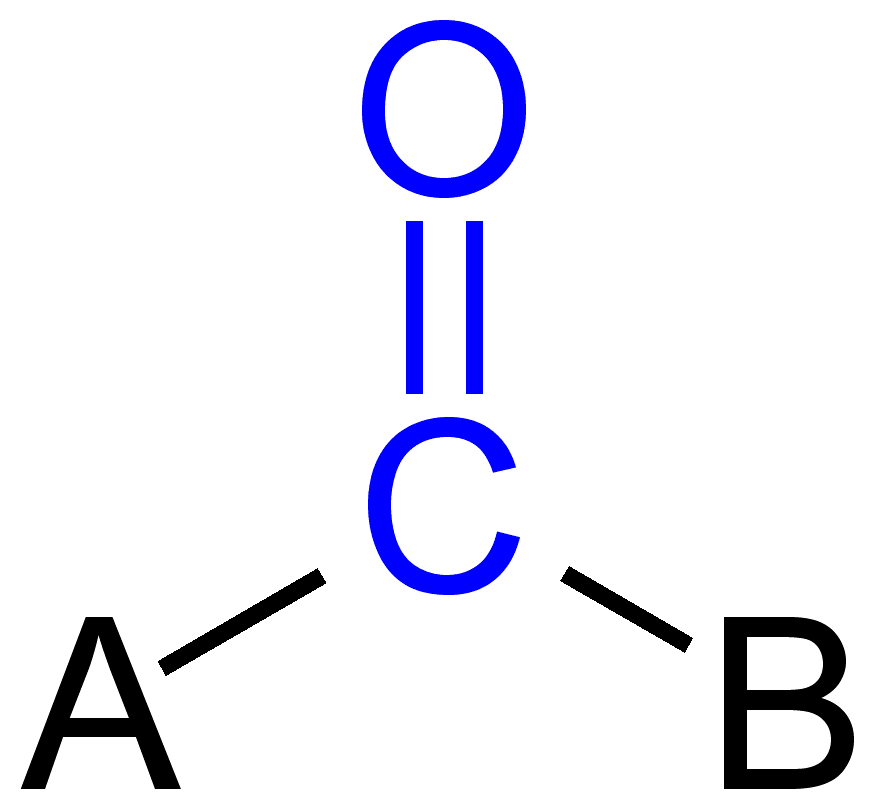
Grupa karbonylowa
Atom węgla grupy karbonylowej ma hybrydyzację sp2 tak więc grupa ma płaską budowę.
Różnica pomiędzy grupą ketonową a aldehydową polega na bezpośrednim wiązaniu się węgla karbonylowego aldehydu z jednym atomem wodoru i jednym atomem węgla, zamiast z dwoma atomami węgla:


Grupa aldehydowa Grupa ketonowa
Związki karboksylowe ze względu na dużą gęstość elektronową na karbonylowym atomie tlenu, mają słabe właściwości zasadowe, jednakże stosunkowo łatwo jest oderwać atom wodoru zlokalizowany w pozycji α od grupy karbonylowej, co nadaje aldehydom i ketonom właściwości kwasowych. Obecność tlenu w grupie karbonylowej wywołuje również jej polaryzację, przez co karbonylowy atom węgla jest podatny na atak nukleofilowy – typowymi dla tych związków reakcjami jest addycja nukleofilowa. Do grupy karbonylowej mogą przyłączyć się alkohol, cyjanowodór, wodorosiarczan (III) sodu, hydrazyna itp.
RCHO + HSO−3 → RCH(OH)SO−3 - addycja wodorosiarczanu (III)
Aldehydy i ketony ulegają również reakcjom redoks, chociaż ketony są mniej reaktywne. Aldehydy można zredukować do alkoholi pierwszorzędowych, natomiast ketony do alkoholi drugorzędowych (aldehydy i ketony uzyskuje się m.in. na drodze utleniania alkoholi):
CH3CHO + H2 → C2H5OH - redukcja aldehydu octowego
Aldehydy ulegają utlenieniu do kwasów karboksylowych w relatywnie łagodnych warunkach:
2CH3CHO + O2 → 2CH3COOH
Dają również pozytywne wyniki prób Tollensa i Trommera:
2[Ag(NH3)2]+ + HCHO + 3OH- → 2Ag↓ + HCOO- + 2H2O + 4NH3 - próba Tollensa
CH3CH2CHO + 2Cu(OH)2 → CH3CH2COOH + Cu2O↓ + 2H2O - próba Trommera
Co więcej, aldehydy ulegają tzw. reakcji Cannizzaro, która jest przykładem dysproporcjonowania (aldehyd ulega jednocześnie utlenieniu i redukcji):

Ketony zdecydowanie trudniej ulegają utlenieniu. Do przeprowadzenia takiej reakcji potrzebne są wyjątkowo silne utleniacze (np. KMnO4) oraz wysoka temperatura. W jej wyniku powstaje mieszanina kwasów karboksylowych. α-hydroksyketony ulegają utlenieniu pod wpływem kwasu jodowego (lub jego soli):
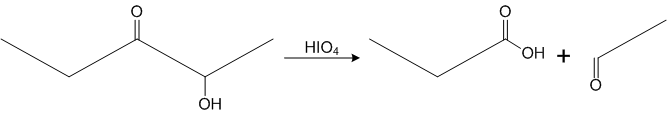
by PabloT99 - Praca własna, CC BY-SA 4.0, https://commons.wikimedia.org/w/index.php?curid=56188502
Aldehydy i ketony reagują również z amoniakiem i aminami dając iminy.
Charakterystyczną dla aldehydów reakcją jest również kondensacja aldolowa tj. połączeniu się dwóch związków karbonylowych, czego produktem są aldole:

Ketony ulegają natomiast reakcji haloformowej, która jest utlenianiem w łagodnych warunkach. Ulegają niej metyloalkilo- i metyloaryloketony.
RCOCH3 + 3NaOX → RCOONa + CHX3 + 2NaOH
Aldehydy to związki toksyczne o właściwościach bakterio- i grzybobójczych. Posiadają charakterystyczne zapachy (przyjemne jak wanilina oraz nieprzyjemne jak formaldehyd). Aldehydy o krótkim łańcuchu węglowym są hydrofilowe. Ketony alkilowe są cieczami, które dobrze rozpuszczają się w wodzie i rozpuszczalnikach organicznych. Są stosowane m.in. jako rozpuszczalniki.
Grupa karbonylowa przy pierścieniu aromatycznym prowadzi do jego dezaktywacji i kieruje kolejne podstawniki w pozycję meta.
Aldehydy i ketony Wasze opinie