Stała dysocjacji to wyrażenie na stałą równowagi dla reakcji dysocjacji. Im stała dysocjacji ma mniejszą wartość tym elektrolit, którego dotyczy, jest słabszy. Stałą dysocjacji oblicza się zgodnie ze wzorem:
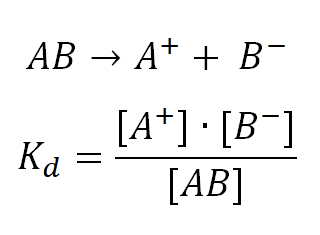
gdzie [A+] i [B-] to stężenie molowe jonów, powstałych podczas dysocjacji, a [AB] - stężenie niezdysocjowanych cząsteczek.
Zadanie
Stężenia jonów oraz cząsteczek niezdysocjowanych w roztworze wodnym pewnego elektrolitu wynoszą kolejno: 0,2M, 0,05M oraz 0,4M. Oblicz stałą równowagi dla tej substancji.
Rozwiązanie
Dane:
[A+] = 0,2M
[B-] = 0,05M
[AB] = 0,4M
Kd = [A+]*[B-] / [AB]
Kd = (0,2*0,05) / 0,4
Kd = 0,025
Odpowiedź: Stała równowagi dla przytoczonego przykładu wynosi 0,025.
Jak obliczyć stała dysocjacji - wyniki